iManage Amblyopia
Projekt-Zusammenfassung
Gesamtziel des Verbundprojekts ist eine interaktive und kontextsensitive Shutterbrille mit sensorischem Feedback zur individualisierten Therapie von Schwachsichtigkeit bei Kindern, die über eine inter-aktive, benutzerfreundliche App für Smartphone und Tablet die Familie des kindlichen Patienten sowie das behandelnde medizinische Fachpersonal in die Verlaufskontrolle und Therapieoptimierung miteinbezieht. Wir streben an, mit diesem körpernahen Medizinsystem die durchschnittliche Tragezeit im Vergleich zur derzeitigen Situation mindestens zu verdoppeln und durch die erhöhte Therapieadhärenz die Zahl der erfolgreichen Therapien deutlich zu erhöhen.
Wussten Sie schon?
Die Amblyopie stellt weltweit eine der häufigsten kindlichen Sehstörungen dar. Die häufigsten Ursachen für die Entwicklung einer Amblyopie sind Refraktionsfehler (Kurz-, Weit- oder Stabsichtigkeit) und Schielfehlstellungen. In der sogenannten „sensitiven Phase“ des Sehens, die bis zum 7. Lebensjahr andauert, reagiert das visuelle System sehr empfindlich auf die Unterdrückung des Seheindruckes. Die Therapie sollte deshalb frühzeitig, also vor dem 7. Lebensjahr begonnen werden, da die Amblyopie in der Entwicklungsphase des Sehens vollständig oder zumindest teilweise reversibel ist.
 Klinischer Hintergrund
Klinischer Hintergrund
Mit einer Prävalenz von 3–5% bildet Schwachsichtigkeit, auch Amblyopie genannt (griech.: stumpfe Sicht), eine der häufigsten Ursachen für Sehbehinderungen während der ersten Lebensjahre. Es handelt sich dabei um eine Unterentwicklung desjenigen Teils des Nervensystems, das für die Verarbeitung visueller Information erforderlich ist. Die Erkrankung kann sich insofern verhängnisvoll auswirken, als sich das lebenslange Risiko einer Erblindung beidseits infolge Erkrankung bzw. Traumatisierung auch des gesunden Auges nahezu verdreifacht. Ursächlich finden sich häufig zunächst organisch bedingte Sehbehinderungen im frühen Kindesalter, wie ein- oder beidseitiger Refraktionsfehler, Schielen oder eine frühkindliche Katarakt. Nach bestmöglicher Korrektur der organischen Ursachen wird die Amblyopie bisher standardmäßig durch Okklusion des besseren Auges mit einem verdunkelnden Pflaster therapiert, wobei der Therapieerfolg von der Okklusionstragezeit abhängt. Als Alternative wird derzeit, mit vielversprechenden Studienergebnissen, auch eine modische elektronische „Shutterbrille“ mit einem LCD-Brillenglas verwendet, mit der das bessere Auge durch Opazifizierung des Brillenglases rhythmisch im 30-Sekunden-Takt okkludiert wird.
Warum sind bestehende Standardtherapien nicht ausreichend?
Die eigentliche Herausforderung in der Therapie besteht per se darin, dass die Therapieadhärenz, insbesondere beim Verdecken des gut sehenden Auges mit einem unbequemen, entstellenden und daher vom Kind schlecht akzeptierten Klebepflaster, sehr unbefriedigend ist. Auch mit den modernen Shutterbrillen ist die Therapieadhärenz, wenngleich besser, häufig noch nicht hinreichend, weshalb unnötig viele Therapien versagen.
Zielsetzung
Bei der im Vorhaben anvisierten interaktiven Shutterbrille handelt es sich um ein unmittelbar am Körper getragenes medizintechnisches System. Die Brille steht in direkter Interaktion mit dem kindlichen Nutzer, indem sie diesem ein direktes, sensorbasiertes Feedback übermittelt und damit sofortige Korrekturmaßnahmen ermöglicht. Eltern und medizinischem Fachpersonal wird täglich ein gebündeltes Feedback bereitgestellt, so dass längerfristig nachhaltige Korrekturmaßnahmen eingeleitet werden können. Außerdem wird die Therapie kontextsensitiv an die jeweilige Situation angepasst. Wir erwarten uns eine deutlich höhere Therapieadhärenz und damit eine bessere Patientenversorgung, wenn das Kind bei falsch sitzender oder abgesetzter Brille durch unmittelbares kindgerechtes Feedback zur Korrektur des Brillensitzes bzw. zum Aufsetzen der Brille motiviert wird, und zusätzlich das Trageverhalten sowie die Zeiten effektiver Okklusion täglich an Eltern und medizinisches Fachpersonal übermittelt und damit überwacht werden können. Die gewonnenen Daten werden darüber hinaus für eine wissenschaftliche Auswertung der Therapie-Compliance eines größeren Patientenkollektivs herangezogen. Die bereits qualitativ festgestellte Dosis-Wirkungsbeziehung ließe sich erstmals wissenschaftlich fundiert quantifizieren.
Wird die Shutterbrille zusätzlich mit Sensorik ausgestattet, lässt sich deren Okklusionsverhalten, abhängig vom jeweiligen situativen Kontext, auch aktiv steuern: Geringe körperliche Aktivität des Kindes erlaubt eine maximale Okklusionsdauer des gesunden Auges zwecks Optimierung des Trainingseffekts für das schwachsichtige Auge, während bei sportlicher Aktivität die Okklusion ausgesetzt werden sollte, um Unfälle aufgrund des sonst fehlenden räumlichen Sehvermögens zu vermeiden.
Wie ist der Projektstand?
Das Vorhaben bekam ein positives BMBF-Votum in der Kategorie „Systemische Umsetzungen und Interaktionskonzepte für eine bessere Handhabung körpernaher Medizintechniksysteme“. Ein Start für die Entwicklung ist mit allen Kooperationspartner, Fraunhofer-Institut für Biomedizinische Technik IBMT und Novidion GmbH, ab April 2017 geplant.
Das Projektteam
Prof. Dr. med. Kai Januschowski (Arbeitsgruppenleiter)
Dr. med. Annekatrin Rickmann (Arbeitsgruppenleiterin)
Prof. Dr. med. Gesine Szurman
Caroline Emmerich
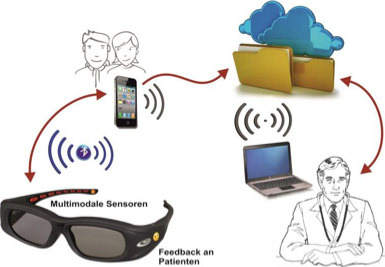 Abbildung: Darstellung des InsisT-Systems. Die mit multimodalen Sensoren und Patientenfeedback ausgestattete Shutterbrille kommuniziert über eine Bluetooth-Schnittstelle bidirektional mit einem Smartphone, wobei die zugehörige Software von den Eltern des Kindes intuitiv bedienbar ist. Das Smartphone übermittelt relevante Daten an eine über das Internet zugängliche Patientenakte, die vom behandelnden Arzt über eine Internetschnittstelle abgerufen und ausgewertet werden kann.
Abbildung: Darstellung des InsisT-Systems. Die mit multimodalen Sensoren und Patientenfeedback ausgestattete Shutterbrille kommuniziert über eine Bluetooth-Schnittstelle bidirektional mit einem Smartphone, wobei die zugehörige Software von den Eltern des Kindes intuitiv bedienbar ist. Das Smartphone übermittelt relevante Daten an eine über das Internet zugängliche Patientenakte, die vom behandelnden Arzt über eine Internetschnittstelle abgerufen und ausgewertet werden kann.
Publikationen
Januschowski K., Bechtold T. E., Schott T. C., Huelber-Januschowski M. S., Blumenstock G., Bartz-Schmidt K. U., Besch D. and Schramm C. (2013). "Measuring wearing times of glasses and ocular patches using a thermosensor device from orthodontics." Acta ophthalmologica 91(8): e635-640.
Januschowski K, Schramm C: Amblyopietherapie im Wandel der Zeit DOG-Symposium (DO26), DOG 2016
Limitations of the TheraMon® -microsensor in monitoring occlusion therapy. Schramm C, Abaza A, Blumenstock G, Bechtold TE, Rickmann A, Bartz-Schmidt KU, Besch D, Januschowski K. Acta Ophthalmol. 2016 Dec;94(8):e753-e756. doi: 10.1111/aos.13134. Epub 2016 Jun 27. PMID: 27350046
Mehr Infos zur interaktiven Shutterbrille
www.insist-brille.de
Stammzelltherapie der Hornhaut
Projekt-Zusammenfassung
Ziel dieser Arbeitsgruppe ist die Etablierung der Isolation von Limbusstammzellen aus Spenderbulbi und der Aufbau einer Kryobank für Limbusstammzellen von HLA-typisierten Spendern, sowie deren Vermittlung. Das Projekt entsteht in einem Europäischen Kryobanking-Verbund zur Kultivierung und Vitrifikation von Limbusstammzellen auf Basis von induzierten pluripotenten Stammzellen (iPS).
Wussten Sie schon?
Die Stammzellen der Limbus corneae Region des Auges dienen als Zellreservoir für Regenerations- und Reparaturprozesse der Hornhaut. Werden diese durch Traumata oder durch Autoimmunerkrankungen zerstört, kann sich die Hornhaut nicht mehr erneuern und Bindehaut sowie Blutgefäße können ungehindert auf der Hornhaut wachsen. Das hat zur Folge, dass sich die Hornhaut eintrübt und die Betroffenen erblinden. Dem Betroffenen kann nur durch eine Transplantation von Limbusstammzellen geholfen werden.
 Klinischer Hintergrund
Klinischer Hintergrund
Die Stammzellen der Limbus corneae Region des Auges, die so genannten Limbusstammzellen, dienen als Zellreservoir für Regenerations- und Reparaturprozesse der Hornhaut. Werden diese durch Traumata (z.B. Verätzungen und Verbrennungen) oder durch Autoimmunerkrankungen mit Bindehaut- und Hornhautbeteiligung zerstört, führt das nicht nur dazu, dass sich die Hornhaut nicht mehr erneuern kann, Bindehaut und Blutgefäße können nun auch ungehindert auf der Hornhaut wachsen. Das hat zur Folge, dass sich die Hornhaut eintrübt und die Betroffenen erblinden. Eine herkömmliche Hornhauttransplantation reicht in diesem Falle nicht aus, da durch sie nicht die zerstörten Limbusstammzellen ersetzt werden und deswegen nach geraumer Zeit die Oberflächenzellen des Hornhauttransplantats ,,aufgebraucht’’ sind. Der Patient erblindet erneut. Das kann durch eine Transplantation von Limbusstammzellen verhindert werden. Da häufig beide Augen betroffen sind, ist eine autologe Transplantation (vom gesunden auf das kranke Auge) meist nicht möglich. Es muss ein Spender gefunden werden, der optimal zu den Gewebemerkmalen des Empfängers passt, um Abstoßungsreaktionen zu vermeiden. Dieser häufig schwierige und langwierige Prozess kann durch eine Limbusstammzellbank mit bereits HLA-typisierten Zellspenden umgangen werden.
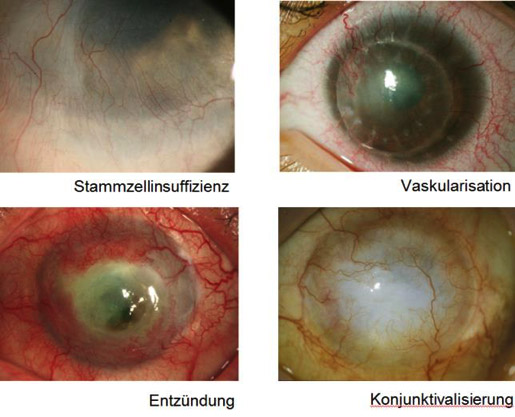
Abbildung: Vier Gründe für eine nicht-erfolgreiche Hornhauttransplantation
Warum sind bestehende Standardtherapien nicht ausreichend?
Gegenwärtig wird eine Limbusstammzell-Insuffizienz in der Regel durch eine autologe Transplantation behandelt. Das bedeutet, dass aus einer gesunden Region im Limbus Stammzellen isoliert und kultiviert werden und in die erkrankte Limbusregion transplantiert werden. In vielen Fällen ist aber die Insuffizienz soweit fortgeschritten, dass nicht genügend gesundes Gewebe bereit steht. Diesen Patienten kann nur durch eine HLA-typisierte Zellspende geholfen werden. Im Gegensatz zu Hornhautspenden gibt es für Limbusstammzell-Spenden keine organisierten Strukturen oder gar Gewebebanken, welche Transplantate vorhalten. Daher gestaltet sich die Spendersuche im Fall von Limbusstammzellen oft schwierig und ist häufig auf die Angehörigen des Patienten beschränkt.
Zielsetzung
Schwerste Hornhauterkrankungen könnten in vielen Fällen schonend mit einer neuen Stammzell-Transplantation behandelt werden. Das Verfahren kommt bei Verätzungen, Verbrennungen und Tumoren in Frage. Wünschenswert ist der Aufbau einer Limbusstammzellbank, welche HLA-typisierte Limbusstammzellen kryokonserviert vorbehält und bei Bedarf an die Transplantationsklinik versendet. Eine Spendersuche wäre in diesem Falle überflüssig und dem betroffenen Patienten könnte umgehend geholfen werden.
 Wie ist der Projektstand?
Wie ist der Projektstand?
Im Mai 2016 wurde in Zusammenarbeit mit der Deutschen Gesellschaft für Gewebetransplantation (DGFG) die Knappschafts-Gewebebank Sulzbach (HSB) eröffnet. Sie erhält aus dem Spendernetzwerk der DGFG humane Spenderbulbi zur Herstellung von Hornhauttransplantaten. Dabei bleibt die Limbusregion der Bulbi als ,,Abfall‘‘ zurück, wodurch auch viele verschiedene Limbusstammzellspenden bereit stehen. Ebenfalls wurde eine Kooperation mit dem Fraunhofer-Institut für Biomedizinische Technik IBMT in Sulzbach ins Leben gerufen, das große Erfahrung in der Kultivierung von Stammzellen und Kryokonserierung mitbringt.
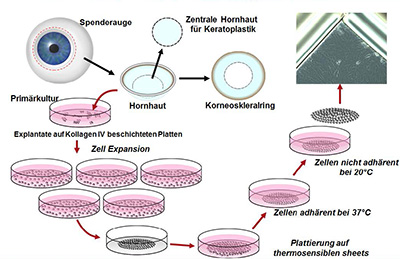
Abbildung: Konzept zur Stammzellgewinnung und Ex-Vivo-Expansion
Das Projektteam
Dr. rer. nat. Silke Wahl (Arbeitsgruppenleiter)
Dr. med. Annekatrin Rickmann
Prof. Dr. med. Peter Szurman
Artificial Cornea
Projekt-Zusammenfassung
Ziel dieser Forschungsgruppe ist die Entwicklung einer mit Tissue Engineering aufgebauten künstlichen Hornhaut, die auf natürlichen, nicht-immunogenen Materialien basiert und in das Empfängergewebe über natürliche Wundheilung stabil einwachsen kann. Grundlegend entwickeln wir dafür eine innovative polymerbasierte 3D-Matrix (folglich mit Zellen beimpft), um somit sowohl anatomische als auch funktionelle Eigenschaften einer primären Hornhaut nachzuahmen.
Wussten Sie schon?
Die Hornhaut hat im Durchschnitt einen Durchmesser von 12 mm und ist 540 Mikrometer (ca. ½ Millimeter) dick. Sie trägt neben ihrer Schutzfunktion mit durchschnittlich 43 Dioptrien zu ¾ der Brechkraft des Auges bei. Der Brechungsindex beträgt 1,367. Aufgrund der fehlenden Blut- und Lymphgefäße ist die Hornhaut immunprivilegiert. Außerdem ist es das dichteste innervierte Gewebe des Körpers.
 Klinischer Hintergrund
Klinischer Hintergrund
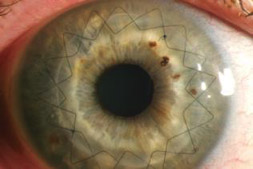
Die Hornhaut-Transplantation ist die älteste, häufigste und erfolgreichste Verpflanzung eines Gewebes beim Menschen. Die erste perforierende Keratoplastik mit mittelfristig klarem Transplantat (über ein Jahr postoperativ) wurde 1905 durchgeführt. Verliert die Hornhaut ihre Transparenz, büßt der Betroffene sein Sehvermögen ein und kann erblinden. Bei einer Hornhautverpflanzung wird die getrübte Hornhaut entfernt und durch die gesunde, klare Hornhaut eines Spenders ersetzt. Eine Trübung der Hornhaut kann viele Ursachen haben. Am häufigsten sind Infektionen, zum Beispiel mit dem Herpesvirus, Verletzungen oder angeborene Erkrankungen. Aber auch extreme Verdünnungen und Verkrümmungen der Hornhaut (z.B. Keratokonus) können eine Transplantation notwendig machen. Bei einer solchen Operation wird der zentrale Teil der natürlichen Hornhaut kreisförmig entfernt und die neue Kornea eingesetzt und vernäht (Abbildung). Die Gefahr einer Abstoßung ist im Vergleich zu einer Organtransplantation zwar relativ gering, denn das durchsichtige Gewebe ist nicht durchblutet, sondern wird per Diffusion mit Nährstoffen versorgt. Trotzdem ist die Zahl der Betroffenen groß. Allein in Europa warten jährlich 40.000 Menschen auf eine Spenderhornhaut.
Warum sind bestehende Standardtherapien nicht ausreichend?
Nicht allen Patienten auf der Hornhaut-Warteliste kann heute geholfen werden, da es nicht genügend Spender gibt. Daraus resultieren lange Wartezeiten für eine Hornhauttransplantation von 3-12 Monaten. Die Fortschritte der letzten Jahre in der Hornhautchirugie und der demografische Wandel werden den Bedarf an Hornhauttransplantaten darüber hinaus weiter steigern. Zusätzlich wird die Zahl der geeigneten Transplante durch die üblichen limitierenden Faktoren, wie Zahl der geeigneten Spender, Vernarbungen der Spenderhornhaut, zu geringe Endothelzellzahl bei Beginn der Kultivierung, positiven virologischen oder mikrobiologischen Befunden und Haltbarkeit der Transplantate, verringert. Daher wurde mit der Zeit auch vermehrt an anderen Techniken zum Ersatz der menschlichen Kornea geforscht, die das Einsetzen nicht kornealen Materials als Hornhautersatz erlaubt. Solche biosynthetischen Keratoprothesen aus Materialien, wie Zahnwurzel, Tibia und Plexiglas machen es möglich, auf Spenderhornhäute zu verzichten. Allerdings lässt sich biologisches Material in der Regel nicht mit dem Körpergewebe fest verbinden und es kann an der Körperoberfläche abgestoßen werden. Darüber hinaus ist die Abbildungsqualität einer natürlichen Hornhaut bedeutend besser.
Zielsetzung
Wünschenswertes Gesamtziel dieses Vorhabens ist die Verbesserung der Bereitstellung von Hornhäuten. Primär soll durch die Entwicklung von artifiziellen Hornhäuten auf polymerbasierter 3D-Matrix erreicht werden, dass mehr Menschen und zeitnah eine angemessene Hornhaut-Transplantation bekommen können und somit deren Sehkraft und folglich auch die Lebenssituation deutlich verbessert werden kann.
Im gesamten pharmazeutischen, medizinischen und toxikologischen Forschungsbereich werden mittlerweile Zellkulturen und Gewebekonstrukte als In-vitro-Modelle und adäquater Ersatz für tierische und humane Gewebe- oder Organsysteme verwendet. Zur Deckung entsprechender Defekte ist hier meist ein Transfer von biologischem Gewebe nötig. Auch Teile der Hornhaut können bereits rekonstruiert werden, beispielsweise mit kultivierten Limbusstammzellen auf Amnionmembran als Trägermatrix. Klinisch wird das bereits bei bestimmten Patienten zur Rekonstruktion schwerer Oberflächenstörungen eingesetzt. Dieses Tissue Engineering der Hornhaut ist Teil eines wachsenden Forschungsgebietes und könnte für die Hornhauttransplantation einen Erfolg versprechenden Ansatz liefern.
 Wie ist der Projektstand?
Wie ist der Projektstand?
Erste erfolgreiche Versuche mit unserem Kooperationspartner, dem Fraunhofer-Institut für Biomedizinische Technik IBMT in Sulzbach, erfolgten auf der Grundlage einer weltweit einmaligen Alginatzusammensetzung. Alle Alginatkonzentrationen konnten sowohl mit als auch ohne Besiedlung von Zellen eine herausragende Transparenz und Stabilität aufweisen (Abbildung). Nach Besiedlung mit kultivierten humanen Keratozyten, die zuvor aus Forschungshornhäuten isoliert wurden, konnten wir über 3 Monate ein langsames Wachstum der Keratozyten beobachten. Wir konnten eine dendritische Netzwerkausbildung und phänotypische Produktion der Extrazellulärmatrix mit Keratocan, Lumican und Kollagen Typ 1 nachweisen.
Wie sind wir methodisch aufgestellt?
Tissue Engineering Methoden zur Synthese von Hornhautkonstrukten, Zellkulturtechniken mit Proliferations- und Toxizitäts-Assays, Biochemische Dezellularisierung von tierischem Gewebe, Endothelzellmessung, Immunfluoreszenz-Aufarbeitung histologischer Gewebeschnitte, Antikörper-Assays, Photometrische Konzentrationsmessung in Gewebe, HPLC, Western-Blot, FACS-Analyse, Gewebepräparation mit Materialgewinnung und Zellzählung und Spezialfärbungen, Vitreoretinale Operationseinheit, Foto, Spaltlampe, Augendruckmessung), Elektrophysiologische Untersuchungseinheit
Das Projektteam
Dr. med. Annekatrin Rickmann (Arbeitsgruppenleiter)
Dr. rer. nat. Silke Wahl
Tisha Stanzel
Prof. Dr. med. Peter Szurman
Kooperationspartner
Fraunhofer-Institut für Biomedizinische Technik IBMT