Superfundiertes isoliertes Netzhautmodell
Projekt-Zusammenfassung
Ziel dieser Arbeitsgruppe ist die elektrophysiologische Untersuchung isolierter Retinakulturen während und nach der Umspülung mit einer Testsubstanz zur Detektion etwaig retinatoxischer Effekte. Hierzu konnten wir ein Organmodell der isolierten superfundierten Netzhautpräparaten aufbauen. Das erlaubt ein in-vivo Monitoring der Netzhautfunktion unter definierter Exposition von zu testenden Wirkstoffen über einen Zeitraum von 36 Stunden. Somit wird ein direktes Monitoring substanzspezifischer Einflüsse auf die Netzhautfunktion ermöglicht. Zusätzlich besteht eine zellbiologische Laborstruktur, die eine standardisierte Bestimmung der selektiven Medikamententoxizität an kultivierten retinalen Zelllinien erlaubt. Seit Bestehen der Arbeitsgruppe haben wir grundlegende Erkenntnisse zum medikamentösen Targeting retinaler Erkrankungen erzielt und damit die klinische Sicherheit neu eingeführter Medikamente verbessert.
Netzhaut - Anatomie & Physiologie
Die Netzhaut befindet sich im hinteren Teil des Auges, in dem die Lichtrezeptoren liegen und die ersten Informationen über das Sehen verarbeitet werden. Sie ist, wie das Gehirn, durch die sogenannte Blut-Retina-Schranke vom restlichen Organismus getrennt.
Als erste Schicht, die das Licht verarbeitet, sind die Photorezeptoren (Stäbchen und Zapfen) zu nennen. Danach schließt sich die äußere plexiforme Schicht an, in der die Fortsätze der Photorezeptoren synaptisch mit den Horizontal- und Bipolarzellen verschaltet sind, die mit den Zellkörpern der Amakrinenzellen die innere Körnerschicht bilden. Weiter nach Innen schließt sich die innere plexiforme Schicht an, in der die Synapsenkontakte der amakrinen Zellen und die der Bipolarzellen mit den Ganglienzellen zu treffen sind. Aus den Axonen der Ganglienzellen wird die Ganglienzellfaserschicht gebildet, die als Nervus opticus zur Sehrinde ziehen. Die Müllerstützzellen bilden die Lamina limitans externa und die Lamina limitans interna.
Die Reiztransduktion in der Netzhaut ist für die Wahrnehmung visueller Reize essentiell und kann zugleich durch Ableitung eines ERGs gemessen werden. Das besondere an den Sinnesrezeptoren der Retina ist, dass Sie im Ruhezustand depolarisiert und im Erregungszustand hyperpolarisiert sind.
Bei anderen neuronalen Mechanismen der Reizverarbeitung im Körper ist das Gegenteil der Fall. Diese Hyperpolarisation ist im ERG messbar.
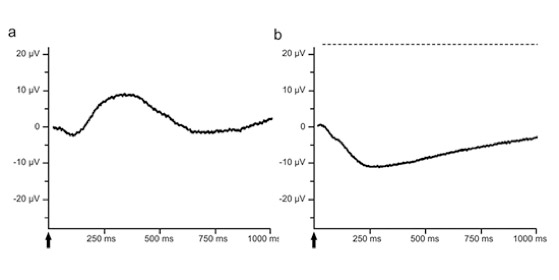
a: Antwort des Photorezeptors im zeitlichen Verlauf dargestellt. Der Lichtreiz ist durch den Pfeil markiert
b: Antwort des höheren neuronalen Netzwerkes im zeitlichen Verlauf dargestellt. Der Lichtreiz ist durch den Pfeil markiert.
Klinischer Hintergrund
Während der Behandlung von Netzhaut- und Glaskörpererkrankungen kommt die Netzhaut nach der Entfernung des natürlichen Glaskörpers (Vitrektomie) mit unterschiedlichen Substanzen in Kontakt. Je nach Krankheitsbild kann auch eine (temporäre) Endotamponade über längere Zeit nach der Operation in der Glaskörperkavität verbleibend. Hierfür müssen diese Substanzen gewisse Voraussetzungen erfüllen. Mithilfe der superfundierten Netzhaut ist es möglich eine potentielle Retinatoxizität vorab zu testen.
Warum sind bestehende Standardtherapien nicht ausreichend?
Aktuell ist es in vitro und in vivo nur leidlich möglich, eine standardisierte Beziehung zwischen Dosis, Applikationszeit und retinaler Toxizität herzustellen. Ein echter in vitro Ansatz ist derzeit aufgrund des komplexen Aufbaus der Retina und deren Störanfälligkeit sowie der fehlenden Perfusion nicht praktikabel.
Zielsetzung
Um den Einsatz von Tierversuchen zu minimieren, verfolgen wir mit der superfundierten Netzhaut einen ex-vivo Ansatz. Hierbei wird eine bovine Netzhaut mit einer Nährlösung und der zu testenden Substanz umspült und im Anschluss eine elektrophysiologische Untersuchungen durchgeführt. Je nach dem Muster der retinalen Antwort auf einen Lichtreiz kann somit auf eine mögliche Retinatoxizität der Substanz geschlossen werden.
So funktioniert das ERG (Elektroretinographie)
Das ERG wurde erstmalig 1849 von Du-Bois-Raymond am Bulbus eines enukleierten Fischauges abgeleitet. Bereits 1945 wurde das ERG klinisch nutzbar gemacht.
Heute ist es der Goldstandard zur Diagnostik bei Netzhautdegenerationserkrankungen oder -dystrophien. Bei einem ERG kann man zwei Wellenkomponenten unterscheiden, eine a-Welle (Hyperpolarisation) und eine b-Welle (Depolarisation). Die a-Welle liefert Informationen über die Funktionalität der Lichtrezeptoren der Netzhaut (Abb. a). Sie ist das durch die Photorezeptoren gebildete Summenpotential, die als erste Antwort auf einen Lichtreiz in Form eines negativen Ausschlags im ERG erscheint. Auf diesen ersten negativen Ausschlag folgt mit einer kurzen Latenz ein positiver Ausschlag, die b-Welle. Von der b-Welle im ERG zieht man Rückschlüsse auf die Funktion der höheren neuronalen Netzwerke innerhalb der Netzhaut (Abb. b). Das Zusammenspiel mehrerer Zelltypen generiert die b-Welle. Sie ist damit als Indikator für die komplexen, integrierenden Netzwerkfunktionen sehr sensibel.
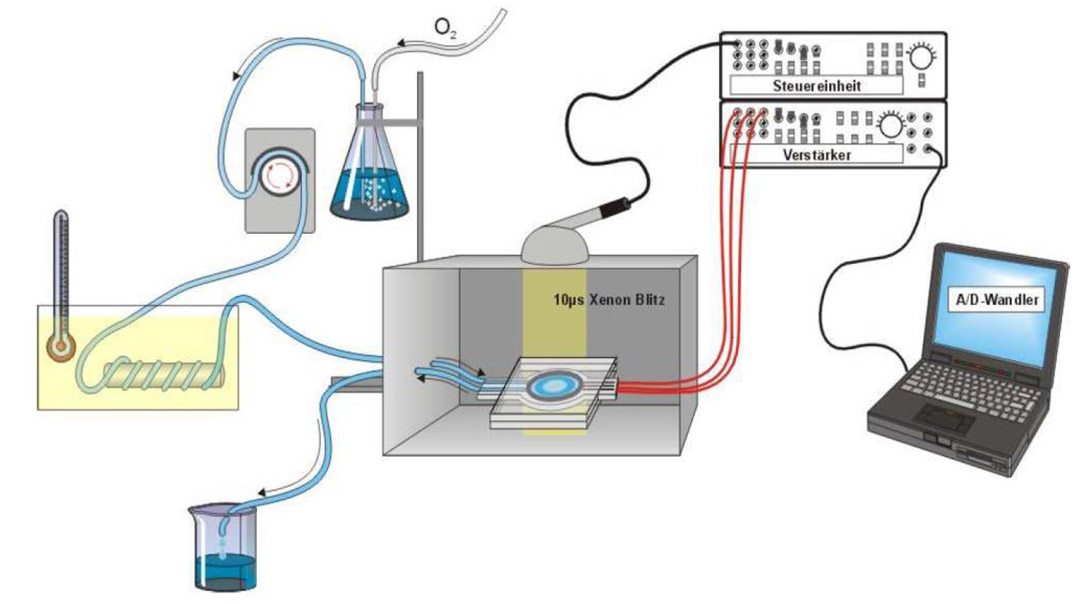
Messung der Retinalen Biokompatibilität
Durch unterschiedliche Reizintensitäten oder durch Zugabe von Aspartat zur Nährlösung können wir die Antwort der Photorezeptoren proportional stärker darstellen oder vollständig isolieren.
Damit lässt sich das Wirkverhalten wie auch der Wirkort verschiedener Substanzen auf die einzelnen Neuronenschichten untersuchen. Wird z.B. eine Verminderung der b-Welle unter Exposition eines Wirkstoffs beobachtet, so kann das an einer Schädigung der Photorezeptoren liegen, die sich dann indirekt auf die Amplitude der b-Welle auswirkt - oder an den Zelltypen, die die b-Welle erzeugen. Mithilfe der separaten Untersuchung von a- und b-Welle können wir das differenzieren. Mit dem ERG hat man ideale Ausgangsbedingungen, um hoch standardisierte Biokompatibiltiätsstudien an einem Organkulturmodel durchzuführen.
Wie ist der Projektstand?
Nach der Etablierung des experimentellen Aufbaus in den letzten Jahren erfolgt nun die kontinuierliche Verfeinerung und Optimierung der Untersuchungsmethode. Die zuverlässige Detektion sowie die präzise Messbarkeit eines möglichen retinatoxischen Effektes konnten wir bereits anhand mehrerer zu untersuchender Substanzen zeigen.
Das Projektteam
Prof. Dr. med. Kai Januschowski (Arbeitsgruppenleiter)
Loic Sermeus
Publikationen
- Januschowski K, Mueller S, Dollinger R, Schnichels S, Hofmann J, Spitzer MS, Bartz-Schmidt KU, Szurman P, Thaler S. Investigating retinal toxicity of tempol in a model of isolated and perfused bovine retina. Graefes Arch Clin Exp Ophthalmol. 2014 Jun;252(6):935-41. doi: 10.1007/s00417-014-2632-4. Epub 2014 May 2. PMID: 24789463
- Januschowski K, Schnichels S, Hagemann U, Koch V, Hofmann J, Spitzer MS, Bartz-Schmidt KU, Szurman P, Lüke M, Aisenbrey S. Electrophysiological toxicity testing of VEGF Trap-Eye in an isolated perfused vertebrate retina organ culture model.Acta Ophthalmol. 2014 Jun;92(4):e305-11. doi: 10.1111/aos.12300. Epub 2013 Nov 8. PMID: 24206925
- Januschowski K, Maddani R, Mueller S, Lueke M, Spitzer MS, Schultheiss M, Bartz-Schmidt KU, Szurman P. Comparing the effects of two different irrigation solutions on an isolated perfused vertebrate retina. Ophthalmic Res. 2012
- Januschowski K, Krupp C, Mueller S, Hofmann K, Schnichels S, Hagemann U, Spitzer MS, Bartz-Schmidt KU, Aisenbrey S. Investigating short-term toxicity of melphalan in a model of an isolated and superfused bovine retina. Graefes Arch Clin Exp Ophthalmol. 2015 Sep 3. [Epub ahead of print] PMID: 26335534
- Januschowski K, Müller S, Krupp C, Spitzer MS, Hurst J, Schultheiss M, Bartz-Schmidt KU, Szurman P, Schnichels S. Glutamate and hypoxia as a stress model for the isolated perfused vertebrate retina. J Vis Exp. 2015 Mar 22;(97). doi: 10.3791/52270. PMID: 25868118
- Januschowski K, Schnichels S, Hagemann U, Koch V, Hofmann J, Spitzer MS, Bartz-Schmidt KU, Szurman P, Lüke M, Aisenbrey S.Electrophysiological toxicity testing of VEGF Trap-Eye in an isolated perfused vertebrate retina organ culture model. Acta Ophthalmol. 2014 Jun;92(4):e305-11. doi: 10.1111/aos.12300. Epub 2013 Nov 8. PMID: 24206925
Suprachoroidale Hydrogelplombe
Projekt-Zusammenfassung
Ziel ist die Entwicklung einer neuen Operationsmethode zur besonders schonenden Behandlung der Netzhautablösung mit einer resorbierbaren Aderhautplombe (AG Experimentelle Retinachirurgie).
Wussten Sie schon?
Die suprachoroidale Hydrogelplombe soll langfristig ein weitverbreitetes Verfahren zur operativen Behandlung der Netzhautablösung werden.
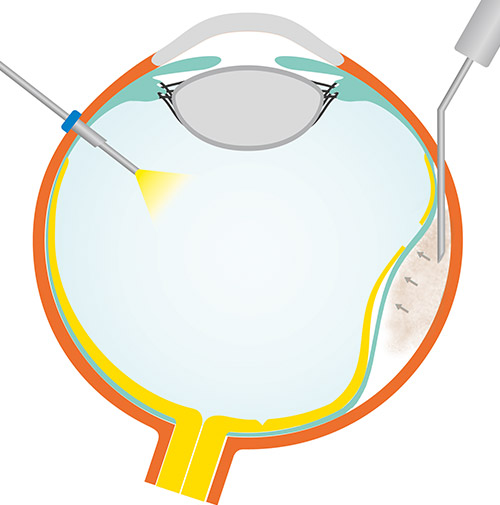 Klinischer Hintergrund
Klinischer Hintergrund
Seit Jules Gonin beruht die Behandlung der Netzhautablösung auf dem Prinzip der Identifikation und des Verschlusses des zugrundeliegenden Netzhautforamens. Sowohl die Buckelchirurgie als auch die Vitrektomie sind hierzu etablierte Verfahren. So unterschiedlich die chirurgischen Ansätze auf den ersten Blick erscheinen, so folgen sie doch beide dem von Custodis 1953 beschriebenen Prinzip der Approximation und Fixation. Entweder geschieht die Approximation und Fixation durch Aufnähen einer skleralen eindellenden Plombe und Fixation mit Kryokoagulation, oder durch eine Vitrektomie mit Approximation durch eine Endotamponade und Fixation durch eine Laserretinopexie.
Warum sind bestehende Standardtherapien nicht ausreichend?
Beide Techniken haben ihre Vor- und Nachteile: Die Buckelchirurgie hat den großen Vorteil der linsenerhaltenden Chirurgie, ist aber technisch veraltet: Sie ist limitiert durch die Verwendung der detailarmen indirekten Ophthalmoskopie, der schlechteren indirekten Illumination und der invasiveren Kryokoagulation. Damit partizipiert sie nicht an den technologischen Errungenschaften, die die moderne Vitrektomie auszeichnen und wird dadurch immer weiter aus der klinischen Routine verdrängt. Umgekehrt profitiert die Vitrektomie von der hochauflösenden Visualisierung mit Weitwinkellupensystemen und hoher Vergrößerung am modernen Mikroskop. Die effektive Endoillumination und schonende Endolaserkoagulation sind weitere Vorteile der Vitrektomie, die zu der hohen Erfolgsrate auch bei schwierigen Ausgangssituationen geführt haben. Allerdings hat die Vitrektomie den großen Nachteil der Notwendigkeit einer Endo-Tamponade mit daraus folgender progressiver Kataraktentwicklung, einer temporären Visusminderung und sonstige Problemen, wie Druckschwankungen als Folge der Tamponade.
 Zielsetzung
Zielsetzung
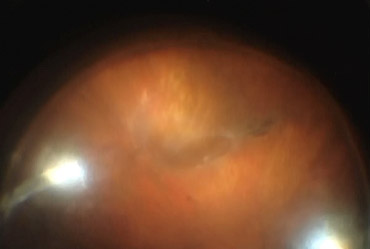
Die suprachoridale Hydrogelplombe soll das Beste aus beiden Welten kombinieren: Die Vorteile der linsenerhaltenden Buckelchirurgie mit gezielter Tamponade des Foramens von außen, aber gleichzeitig die Verwendung der modernen ophthalmochirurgischen Techniken mit Weitwinkelvisualisierung, Endoillumitation und Endolaser. Zusätzlich besteht der Anspruch an eine solche minimal-invasive Technik, dass sie einfach und schnell durchführbar ist, ohne eine großflächige Peritomie der Bindehaut auskommt, buckelassoziierte Probleme wie postoperative Doppelbilder oder eventuelle Plombendurchwanderung vermeidet. Insbesondere Lochsituationen im Bereich der Augenmuskeln sollten diese nicht mechanisch kompromittieren oder zu intraoperativen Schwierigkeiten führen.
Abbildung: Buckeleffekt der Hydrogelplombe intraoperativ
Wie ist der Projektstand?
Die suprachoroidale Hydrogelplombe konnte erstmals 2015 als neues, einfaches und sicheres Verfahren zur Behandlung der Netzhautablösung vorgestellt werden. Die technischen Vorteile der modernen Vitrektomie und der klassischen Buckelchirurgie werden in diesem operativen Ansatz vereint werden. Die Technik lässt sich additiv in Kombination mit der Vitrektomie oder als „stand-alone procedure“ angewenden. Als geeignetes Tamponadematerial hat sich das quervernetzte Hydrogel mit einer Resorptionsdauer von bis zu 8 Wochen herausgestellt. Es werden noch weitere Untersuchungen mit Langzeiterfahrungen empfohlen, die zu einer weiteren Verbreitung der suprachoroidalen Hydrogelplombe als operatives Verfahren zur Behandlung der Netzhautablösung führen sollen.
Das Projektteam
Prof. Dr. med. Peter Szurman (Arbeitsgruppenleiter)
Prof. Dr. med. Kai Januschowski
PD Dr. med. Karl Boden
Femtosekundenlaser
Projekt-Zusammenfassung
Als Referenzzentrum für den FEMTO LDV Z8 sind wir an einem hohen Qualitätslevel im Umgang mit Femtosekundenlaser in der Ophthalmochirurgie interessiert. Zusätzlich möchten wir zur Weiterentwicklung der Femtosekunden-Lasertechnologie zur schonenden Laseroperation an der Hornhaut und der Linse beitragen und sind Europäisches Referenzzentrum für diese revolutionäre Technik.
Wussten Sie schon?
Femtosekundenlaser sind Infrarotlaser mit einer sehr geringen Pulsenergie von 10-15 Joul (Nanojoul-Bereich). Sie arbeiten über den Mechanismus der Photodisruption. Das Prinzip ist dem des Nanosekunden Nd-YAG-Lasers sehr ähnlich. Der fokussierte Puls des Lasers erzeugt ein Plasma mit freien Elektronen und ionisierten Molekülen, die eine Stoßwelle erzeugen. Die Kavitation erzeugt dann eine Gasblase, die sich expandiert bevor sie wieder zusammenbricht, was zu einer Aufspaltung von Gewebe führt. Durch die Aneinanderreihung einzelner Laserpulse entsteht das gewünschte Lasermuster. Der Einsatz sehr kleiner Laserspots mit ultrakurzer Pulsrepetitionsrate (>5 MHz) kann dabei den Umfang der lokalen Nebenwirkungen, wie die Entstehung mechanischen Stresses, deutlich reduzieren - bei gleichzeitig erhöhter lokaler Effektivität.
 Klinischer Hintergrund
Klinischer Hintergrund
In den letzten Jahren hat sich der Einsatz von lasergestützten Operationsverfahren in der Ophthalmochirurgie immer stärker etabliert. Dabei lassen sich einzelne Operationsschritte, etwa in der Kataraktchirurgie, mithilfe des Femtosekundenlasers bewerkstelligen. Hierzu zählen die Anlage der Inzisionen als Operationszugang, die Zerteilung des Linsenkerns und die Kapsulotomie. Diese werden jeweils mithilfe eines intraoperativ verwendeten OCTs individuell abgestimmt.
Abbildung: Der mobile Niedrigenergie Femtosekundenlaser FEMTO LDV Z8 (Ziemer Ophthalmic Systems AG, Port, Schweiz).
Warum sind bestehende Standardtherapien nicht ausreichend?
Die Femtosekundenlaser assistierte Kataraktoperation hält zunehmend Einzug in die moderne Ophthalmochirurgie. Als potenzielle Vorteile gegenüber der manuellen Kataraktoperation werden die höhere Standardisierbarkeit sowie Reproduzierbarkeit der Schnittführung und der Kapseleröffnung mit einer kreisrunden Kapsuolotomie gesehen. Durch den Einsatz des Femtosekundenlasers zur Kernfragmentierung können wir die dabei erforderliche Ultraschallenergie deutlich verringern oder deren Einsatz teilweise sogar ganz vermeiden.
Zielsetzung
Als Referenzzentrum für die Anwendung des LDV Z8 möchten wir zu einer einfachen und zuverlässigen Anwendung des Niedrigenergielasers beitragen. Ziel ist dabei die Auswertung klinischer Daten wie auch Ergebnisse präklinischer Untersuchungen zur weiteren Standardisierung und Optimierung der Femtosekundenlaser assistierten Kataraktchirurgie.
Wie ist der Projektstand?
Seit 2014 werden Femtosekundenlaser assistierte Kataraktoperationen mit dem FEMTO LDV Z8 an unserer Klinik durchgeführt. Klinische Daten bestätigen eine sichere und standardisierte Anwendung des Femtosekundenlasers. Präklinische wie auch klinische Untersuchungen ergeben dabei neue Erkenntnisse auf dem Feld der lasergestützten Kataraktchirurgie.
Das Projektteam
PD Dr. med. Karl Thomas Boden (Arbeitsgruppenleiter)
Prof. Dr. med. Kai Januschowski
Dr. med. Katrin Boden
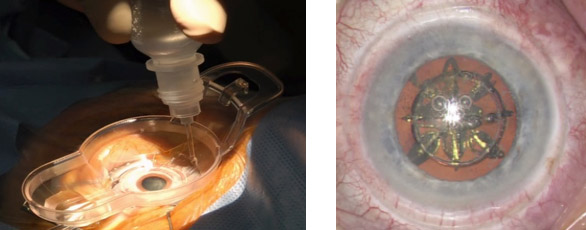
Durchführung einer Femtosekundenlaser assistierten Kataraktoperation (links: das Liquid Patient Interface; rechts: Kernteilung nach Femtosekundenlaser assistierter Fragmentierung)